13 Dic El punto triple del CO2 bióxido de carbono
A la convergencia entre los estados sólido, líquido y gaseoso de una sustancia se le llama “punto triple” y ocurre cuando se modifica la relación entre la presión y la temperatura.
El dióxido de carbono requiere cualidades muy distintas a los otros refrigerantes para evitar que alcance esta condición.
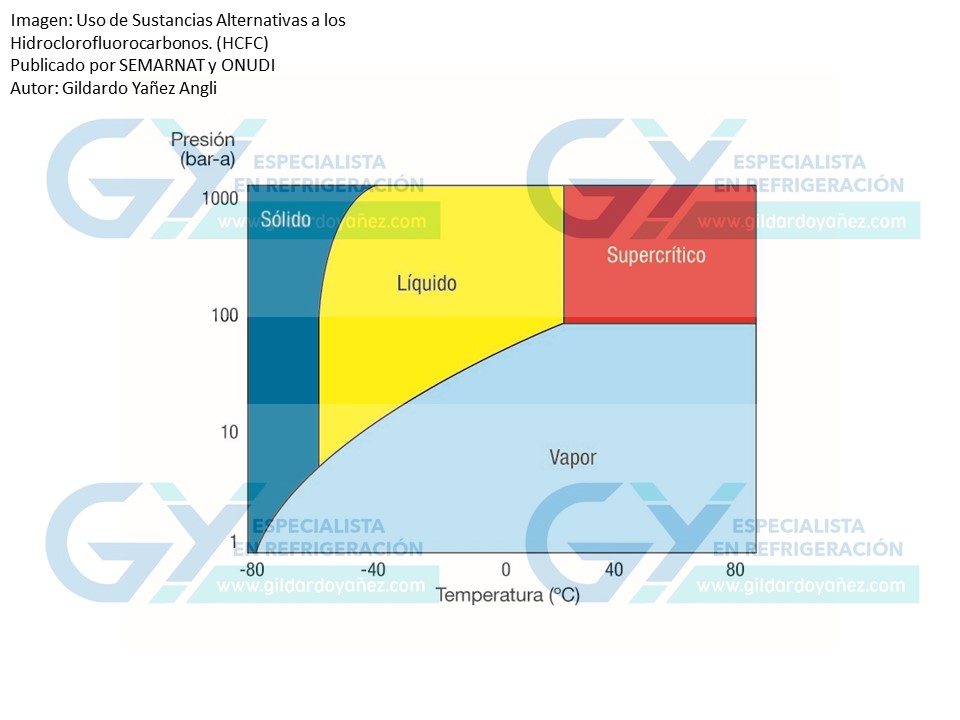
- El punto triple del CO2 es la condición en la que el estado sólido, líquido y gaseoso coexisten.
- En la imagen se observa el estado del CO2 cuando alcanza este punto.
- Presión 5.2 bar-a / Temperatura -56.6°C
Normalmente, cuando se utiliza el dióxido de carbono como refrigerante requiere una presión mayor que los hidrofluorocarbonos y otros refrigerantes. Esta condición conlleva algunos problemas, pero, por lo general, éstos pueden ser superados con un diseño de sistemas específico para el uso de dióxido de carbono. Es necesario recordar que el punto crítico de un refrigerante se presenta en el momento en que aumenta la temperatura o la presión y esto ocasiona que no sea posible lograr la condensación del refrigerante. En el punto crítico las densidades del gas y del líquido son iguales, más allá de este punto, las fases de vapor y líquido no existen. Por mucho que se comprima el gas, este ya no se puede condensar.
Debido a que el punto crítico del CO2 se produce con una baja temperatura, el punto triple en una instalación puede aparecer. En sistemas de refrigeración pueden coexistir los estados sólido, líquido y gaseoso del refrigerante. Esta situación se puede presentar al bajar súbitamente la presión del sistema (fuga). El punto triple del CO2 se presenta a los -56.56 °C.
La gran diferencia entre el CO2 y los refrigerantes sintéticos es su relación presión / temperatura y, particularmente, su alta presión a temperaturas normales y su baja temperatura crítica de aproximadamente 31 ºC.
Esta distinción es notable debido al valor del punto triple del CO2, el cual es superior respecto de otros refrigerantes.
El punto triple del CO2 en valores teóricos se presenta con una presión de 75.124 psia (5.111 atm) y una temperatura de -69.80 ºF (-56.56 ºC). En este punto, las fases vapor, líquido y sólido están en equilibrio. Mientras que la presión crítica teórica del CO2 es de 1070.0 psia (72.808 atm) y la temperatura crítica de 87.76 ºF (30.97 ºC).
En conclusión, el encuentro de las tres fases de la materia, producido por el equilibrio termodinámico entre el estado sólido, líquido y gaseoso de una sustancia, es conocido como punto triple. Éste se origina conjugando los niveles de temperatura y presión con los cuales se produce cada uno de los estados de una sustancia o materia.
Video: Demostración de los tres cambios de fase del dióxido de carbono

